新聞網(wǎng)訊 一個(gè)世紀(jì)之前,德國(guó)生物化學(xué)學(xué)家Otto Warburg發(fā)現(xiàn)腫瘤細(xì)胞即使是在氧氣充足情況下�,優(yōu)先選擇通過(guò)糖酵解而不是三羧酸循環(huán)獲取能量,即Warburg效應(yīng)���。
8月6日�����,我校腫瘤精準(zhǔn)醫(yī)學(xué)研究院的孫鵬博士���、馬蕾娜副教授和呂志民教授在Cell子刊Cell Metabolism(影響因子27.7)上發(fā)表了題為“Lactylation: Linking the Warburg effect to DNA damage repair”的評(píng)述����。闡述了Warburg效應(yīng)通過(guò)乳?��;{(diào)控DNA損傷修復(fù)的關(guān)鍵機(jī)制���。
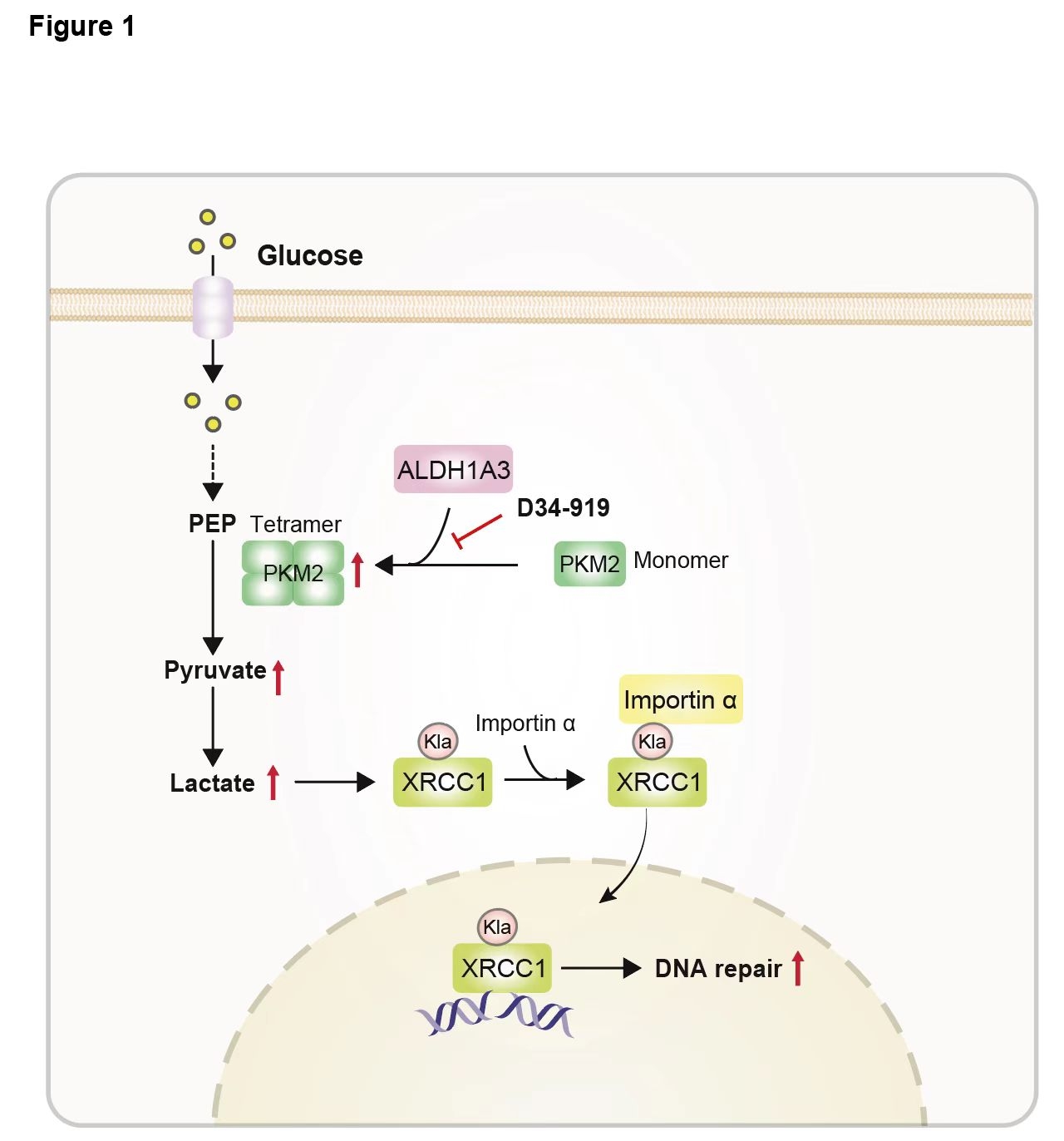
北京天壇醫(yī)院張偉教授和江濤院士在同期的CellMetabolism雜志上發(fā)表了題為Glycometabolicreprogramming-induced XRCC1lactylationconfers therapeutic resistance in ALDH1A3-overexpressing glioblastoma的研究論文。呂志民教授應(yīng)邀對(duì)這一發(fā)現(xiàn)做了重要總結(jié)與評(píng)述�。該評(píng)述指出,Warburg效應(yīng)不僅僅是一個(gè)代謝現(xiàn)象����,其對(duì)多種非代謝細(xì)胞活動(dòng)具有關(guān)鍵影響。本研究揭示了非糖酵解酶ALDH1A3與PKM2的相互作用增強(qiáng)糖酵解和乳酸生成的機(jī)制����,并展示了Warburg效應(yīng)通過(guò)乳酸介導(dǎo)的蛋白乳酰化調(diào)控DNA損傷修復(fù)的全新發(fā)現(xiàn)。干預(yù)這一過(guò)程在提高膠質(zhì)母細(xì)胞瘤對(duì)DNA損傷誘導(dǎo)療法的敏感性方面具有令人期待的潛力��。
孫鵬博士和馬蕾娜副教授為本文共同第一作者���。該工作得到科技部重點(diǎn)研發(fā)計(jì)劃���、國(guó)家自然科學(xué)基金��、國(guó)家生物藥創(chuàng)新中心揭榜掛帥項(xiàng)目的資助��。
原文鏈接:
https://authors.elsevier.com/c/1jYkN5WXUlWkET






![]() 魯公網(wǎng)安備 37021202000856號(hào)
魯公網(wǎng)安備 37021202000856號(hào) ![]()